-
12
10月

Nat Biotechnol发表基于纳米孔的tRNA直接测序新方法
RNA是存在于生物细胞以及部分病毒、类病毒中的遗传信息载体,不同类型RNA具有不同的作用。转移RNA(tRNA)在蛋白质翻译中起着重要作用。如果tRNA中发生错误修饰或修饰缺失,会产生错误或不完整的蛋白质。
已有研究发现,多种tRNA修饰酶的突变与各种人类疾病有关,包括神经退行性疾病、代谢疾病和癌症。但是,研究tRNA一直面临着诸多挑战,部分原因是缺乏一种同时量化其丰度和化学修饰的简单方法。因为目前的纳米孔测序设置会丢弃绝大多数tRNA reads,测序产量低,并且基于转录物长度对tRNA丰度的表示有偏差。
近日,来自西班牙巴塞罗那科学技术研究所的研究团队及合作者在Nature Biotechnology发表了题为“Quantitative analysis of tRNA abundance and modifications by nanopore RNA sequencing”的研究论文。研究团队开发了一种名为Nano-tRNAseq的tRNA纳米孔测序新方法,可直接对天然tRNA进行精确测序,准确定量tRNA丰度并同时捕获tRNA修饰变化。研究团队利用Nano-tRNAseq成功检测了酿酒酵母tRNA群同一分子内不同tRNA修饰类型之间的串扰和相互依赖性,以及tRNA群体对氧化应激的反应变化。

图1.文章发表在Nature Biotechnology
牛津纳米孔技术公司(ONT)开发的直接RNA测序(DRS)平台是基于NGS技术来描述tRNA组的一个很有潜力的替代方案。该技术允许对天然RNA分子进行直接测序,因此,原则上可以检测和定量tRNA修饰和tRNA丰度,不需要逆转录或PCR。先前的研究已经证明,纳米孔可以使用固态或生物(ONT)纳米孔捕获tRNA。通过连接接头来延长tRNA分子,tRNA可以通过生物纳米孔进行测序、基础标记和定位。但上述方法tRNA分子的测序产量较低,并且没有报告是否使用该方法再现了现存的体内tRNA丰度和/或tRNA修饰。
研究团队发现,对原始纳米孔信号强度再处理,用RNA接头填充5′和3′tRNA末端,可以准确地进行碱基判定和映射,并捕获整个tRNA序列,使tRNA reads的数量增加12倍,并获得准确的tRNA丰度。这种基于纳米孔的方法被命名为Nano-tRNAseq(图1),可用于对天然tRNA进行测序,并在单个实验中获取到tRNA丰度和修饰动力学的定量估计。研究团队表示,在体外和天然tRNA分子测序、碱基判定和映射方面,Nano-tRNAseq方法是使用纳米孔进行DRS最成功的方法。
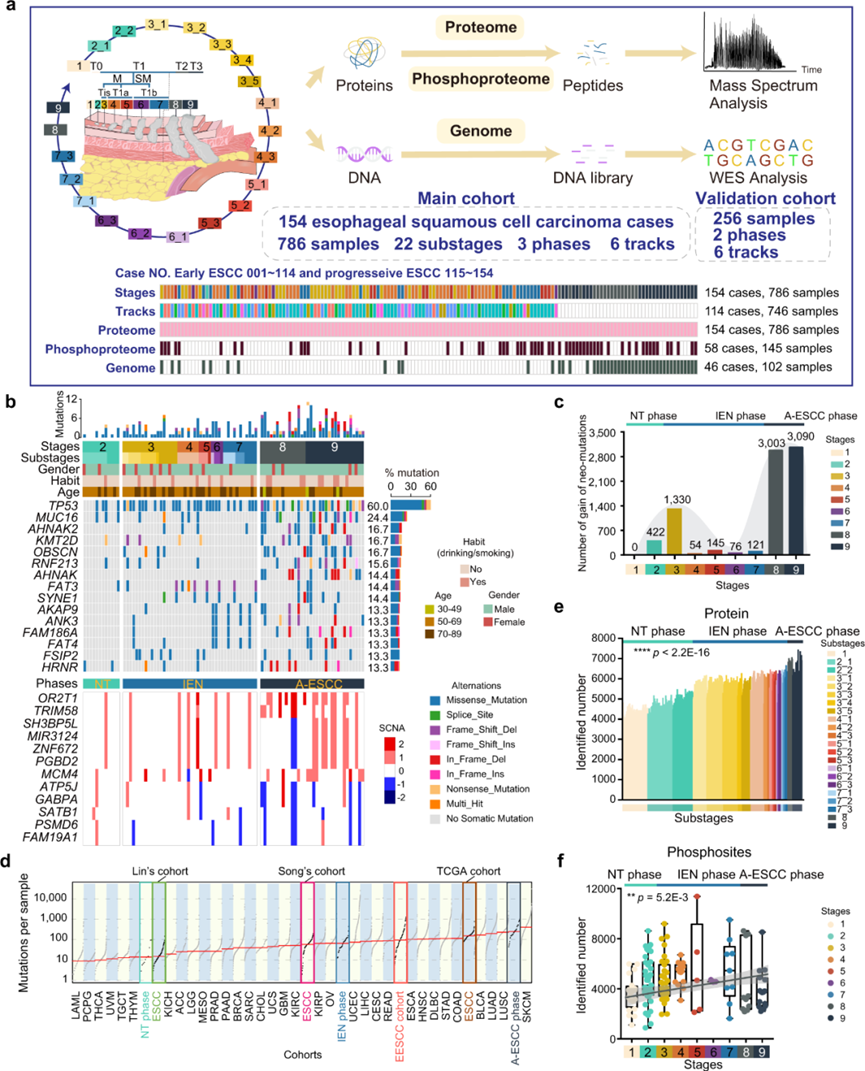
图2.Nano-tRNAseq可以有效地对天然tRNA进行测序
天然tRNA具有短而高度修饰的特性,这使它们的比对具有挑战性。对DRS数据集中修改碱基的不准确判定也使原tRNA检测含有很大比例的不匹配碱基。由于这些错误的碱基,使用推荐设置的常用长读长映射工具minimup2(-ax-map ont-k15)仅可以比对一小部分reads(2.56%)。为了提高Nano-tRNAseq reads可映射性,研究团队测试了短reads映射算法BWA,发现使用推荐参数的BWA-MEM比对在映射readas的比例方面优于minimup2。
当使用参数为-W13 -k6 -xont2d -T20的BWA-MEM时,发现增加的映射reads和错误比对之间存在最佳平衡,映射了54.63%的reads,错误比对很少(0.19%)。当在天然tRNA分子中比较两个映射算法的性能时,对比更加明显。随后,研究人员评估了Nano-tRNAseq reads的可映射性是否受5'和3' RNA接头长度的影响。研究发现,即使参考序列中没有RNA接头,短的和未修饰的序列也可以有效地比对,而短的和修饰的reads则从带有接头的延伸序列中受益匪浅,表明带有RNA接头的延伸序列分子对于指导富含“错配”短reads的正确比对至关重要,例如来自天然tRNA的短reads。
-
01
09月

Molecular Cell | 西湖大学施一公团队再获新进展!解析人类pre-tRNA剪接机制,完善剪接体结构
该研究的人类TSEN/CLP1/pretRNA复合物在催化前和催化后状态下的结构为理解pre-tRNA剪接的机制提供了一个框架。 从tRNA前体 (pre-tRNA)中去除内含子在生命的三个王国中都是必不可少的。在人类中,这一过程是由tRNA剪接内切酶(TSEN)介导的,包括四个亚基:TSEN2、TSEN15、TSEN34和TSEN54。
2023年4月6日,西湖大学施一公团队在Molecular Cell (IF=19)在线发表题为“Structural basis of pre-tRNA intron removal by human tRNA splicing endonuclease”的研究论文,该研究揭示了人tRNA剪接核酸内切酶去除tRNA前体内含子的结构基础。该研究报道了人TSEN在催化前和催化后的平均分辨率分别为2.94和2.88 Å下与全长pre-tRNA结合的冷冻电镜结构。
人体TSEN具有一个延伸的表面凹槽,容纳l型的pre-tRNA。pretRNA的成熟结构域由TSEN34、TSEN54和TSEN2的保守结构元素识别。这种识别定位pre-tRNA的反密码子茎,并将30剪接位点和50剪接位点分别放置在TSEN34和TSEN2的催化中心。大部分内含子序列与TSEN没有直接的相互作用,这解释了为什么不同内含子的pre-tRNAs可以被容纳和裂解。该结构揭示了TSEN pre-tRNA裂解的分子尺机制。
转运RNA (tRNA)对于遗传信息的流动至关重要,它允许核糖体将mRNA翻译成蛋白质。成熟tRNAs是由tRNAs前体 (pre-tRNAs)通过一系列转录后处理和修饰步骤生成的。在生命的三个王国中,对于pre-tRNAs的一个子集,内含子序列都存在,必须通过剪接去除。在人类基因组中预测的tRNA基因中,至少有28个含有长度和序列不同的内含子。在古生菌和真核生物中,内含子通过tRNA剪接内切酶(TSENs)去除,然后通过涉及特定tRNA连接酶的多步骤过程连接两个释放的外显子。
真核生物TSEN包括两个催化亚基TSEN34和TSEN2,两个结构亚基TSEN54和TSNE15,TSEN34和TSEN2分别在30剪接位点(30SS)和50剪接位点(50SS)切割pre-tRNA。在哺乳动物中,多核苷酸激酶CLP1与TSEN共纯化。尽管CLP1在体外tRNA切割前是可有可无的,但CLP1和所有TSEN亚基的突变已与tRNA代谢改变和神经病变相关。
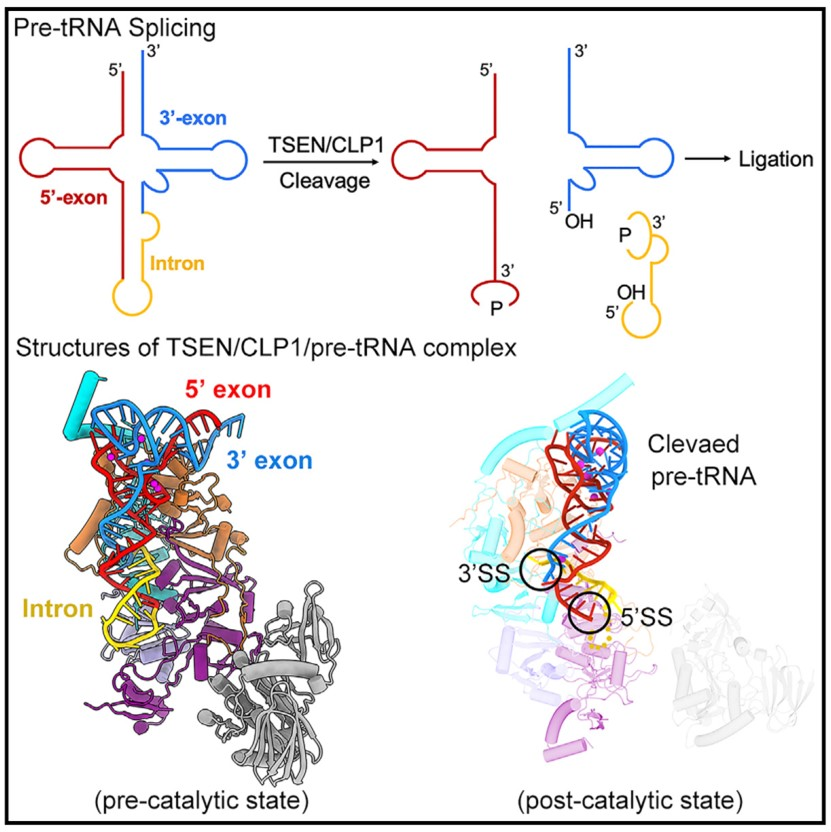
机理模式图(图源自Molecular Cell )
自从20世纪70年代发现tRNA内含子以来,广泛的生化和晶体学研究中对各种类型的TSENs的pre-tRNA裂解有了相当大的了解。特别地,古生菌TSEN与隆起-螺旋-隆起(BHB) RNA基序复合物的结构揭示了一些关键的相互作用,这些相互作用是pre-tRNA识别和切割所必需的。然而,关于真核生物TSEN的结构信息出现缓慢,严重限制了对pre-tRNA裂解机制的理解。例如,TSEN被认为采用分子尺机制来识别pre-tRNA的两位点切割,但由于缺乏被TSEN结合的全长pre-tRNA的结构信息,其基础仍不充分。此外,四个TSEN亚基是如何被组织成一个完整的、具有两个独立活性位点的内切酶的仍不清楚。
该研究报道了人类TSEN与全长pre-tRNA结合的两个高分辨率结构:一个处于催化前状态,另一个处于催化后状态。为了捕捉预催化状态,作者在TSEN中引入了两个错意突变:TSEN34中的H255A和TSNE中的H377A。
总之,该研究的人类TSEN/CLP1/pretRNA复合物在催化前和催化后状态下的结构为理解pre-tRNA剪接的机制提供了一个框架。